新闻动态
3D打印DNA涂层“化学过滤器”解锁靶向癌症治疗
更新时间:2021-06-29 09:36:21
加州理工学院和加州大学旧金山分校的科学家开发了载有 DNA的3D打印结构,能够将化疗药物引导至受影响的器官并远离健康组织。绰号“化学过滤器”的新型设备可以在动脉内化疗期间注射到患者体内,以排出受影响的器官并防止有毒物质进入他们的血液。由于其基因组 DNA 涂层,该团队表示,ChemoFilters 能够高效捕获阿霉素,并使患者免受脱靶毒性的副作用。

该团队 3D 打印的药物吸收剂的 SEM 图像。通过用基因组 DNA 涂覆他们的设备,该团队能够赋予它们吸收药物的特性。图片来自应用材料和界面杂志。
化疗过滤创新
根据美国癌症协会的一项研究,到 2040 年,癌症死亡人数将达到 1600 万,这一统计数据令人怀疑当前治疗方法的有效性。虽然化疗已成为对抗疾病的有力工具,但其成功仍受到“全身毒性”的限制,这种现象是癌细胞未被吸收的药物反而杀死健康细胞,通常会导致器官损伤。更糟糕的是,许多化疗药物在更高剂量下表现出更大的功效,迫使临床医生在最大限度地抑制肿瘤和避免对周围组织造成损害之间做出选择。在开发出更有针对性的治疗方法的地方,它们也伴随着冗长的研发时间以及其他使人衰弱的副作用,这可能使患者无法接受治疗。
为了解决这个问题,加州大学旧金山分校的科学家们在 2014 年首次创建了化学过滤器,它被包裹在外部 DNA 中,这样化学药物就会攻击它们而不是健康细胞,但是尽管尝试对团队的初始设计进行迭代,但存在局限性药物结合材料的使用阻碍了升级设备的生产。最近,附近的加州大学伯克利分校的研究人员发现,磺化 3D 打印共聚物具有出色的药物捕获潜力。从他们的同胞的成功中汲取灵感,加州理工学院和加州大学旧金山分校的团队现在提出用 DNA 涂覆聚丙烯酸酯,可以使它们在体外药物捕获应用中更加有效。
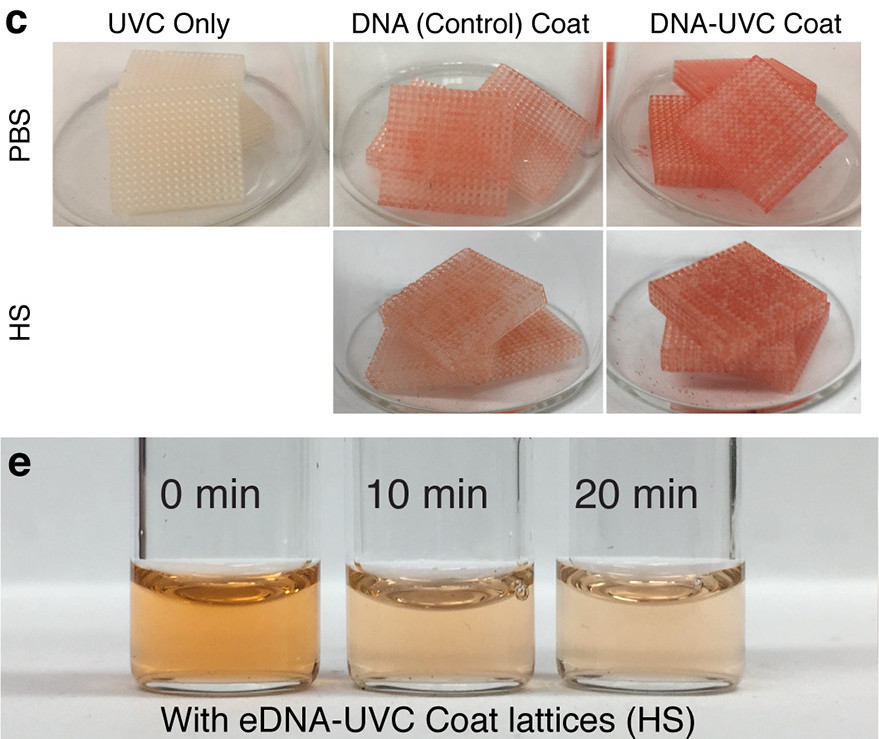
研究人员 3D 打印了 DNA 加载和控制部件。该团队发现静电相互作用是实现 DNA 结合的最有效方法。图片来自应用材料和界面杂志。
载有 DNA 的“化学过滤器”
首先,科学家们使用 Autodesk Ember DLP 3D 打印机和 PR48 树脂来生产一组 12 毫米(宽)x 2.5 毫米(高)立方晶格。每个设备具有 16 x 16 x 3 内部单元,开口约为 500 μm,使其足够大以允许细胞流过,并且它们的整体结构足够小以进行体外部署。准备就绪后,该团队使用两种不同的技术用基因组 DNA 涂覆他们的部件。在第一种方法中,未经处理的晶格被浸泡在酸性 DNA 溶液中,而第二种方法是研究人员将静电相互作用和 UVC 交联结合起来,将带负电荷的基因组结合到他们的设备上。
在科学家们甚至开始测试之前,他们就知道前者导致 DNA 链聚集成纤维团而不是覆盖晶格表面,从而导致层数减少。为了最大限度地提高其设备的药物吸收性能,并防止潜在的 DNA“泄漏”,该团队因此在测试前将它们浸泡在 PBS 中,在此期间,他们在体外条件下将它们暴露于阿霉素。与普通晶格相比,研究人员的新型设备证明能够捕获几乎两倍数量的抗癌药物,每 30 分钟浸出每平方毫米材料 100 pg 基因组 DNA,导致团队得出结论,它们代表了“朝着将这些设备转化为临床应用。”

该团队 3D 打印的药物吸收剂的 SEM 图像。通过用基因组 DNA 涂覆他们的设备,该团队能够赋予它们吸收药物的特性。图片来自应用材料和界面杂志。
化疗过滤创新
根据美国癌症协会的一项研究,到 2040 年,癌症死亡人数将达到 1600 万,这一统计数据令人怀疑当前治疗方法的有效性。虽然化疗已成为对抗疾病的有力工具,但其成功仍受到“全身毒性”的限制,这种现象是癌细胞未被吸收的药物反而杀死健康细胞,通常会导致器官损伤。更糟糕的是,许多化疗药物在更高剂量下表现出更大的功效,迫使临床医生在最大限度地抑制肿瘤和避免对周围组织造成损害之间做出选择。在开发出更有针对性的治疗方法的地方,它们也伴随着冗长的研发时间以及其他使人衰弱的副作用,这可能使患者无法接受治疗。
为了解决这个问题,加州大学旧金山分校的科学家们在 2014 年首次创建了化学过滤器,它被包裹在外部 DNA 中,这样化学药物就会攻击它们而不是健康细胞,但是尽管尝试对团队的初始设计进行迭代,但存在局限性药物结合材料的使用阻碍了升级设备的生产。最近,附近的加州大学伯克利分校的研究人员发现,磺化 3D 打印共聚物具有出色的药物捕获潜力。从他们的同胞的成功中汲取灵感,加州理工学院和加州大学旧金山分校的团队现在提出用 DNA 涂覆聚丙烯酸酯,可以使它们在体外药物捕获应用中更加有效。

研究人员 3D 打印了 DNA 加载和控制部件。该团队发现静电相互作用是实现 DNA 结合的最有效方法。图片来自应用材料和界面杂志。
载有 DNA 的“化学过滤器”
首先,科学家们使用 Autodesk Ember DLP 3D 打印机和 PR48 树脂来生产一组 12 毫米(宽)x 2.5 毫米(高)立方晶格。每个设备具有 16 x 16 x 3 内部单元,开口约为 500 μm,使其足够大以允许细胞流过,并且它们的整体结构足够小以进行体外部署。准备就绪后,该团队使用两种不同的技术用基因组 DNA 涂覆他们的部件。在第一种方法中,未经处理的晶格被浸泡在酸性 DNA 溶液中,而第二种方法是研究人员将静电相互作用和 UVC 交联结合起来,将带负电荷的基因组结合到他们的设备上。
在科学家们甚至开始测试之前,他们就知道前者导致 DNA 链聚集成纤维团而不是覆盖晶格表面,从而导致层数减少。为了最大限度地提高其设备的药物吸收性能,并防止潜在的 DNA“泄漏”,该团队因此在测试前将它们浸泡在 PBS 中,在此期间,他们在体外条件下将它们暴露于阿霉素。与普通晶格相比,研究人员的新型设备证明能够捕获几乎两倍数量的抗癌药物,每 30 分钟浸出每平方毫米材料 100 pg 基因组 DNA,导致团队得出结论,它们代表了“朝着将这些设备转化为临床应用。”
该团队在他们的论文中总结道:“通过设备方法减少化疗中的脱靶毒性具有巨大的意义,并有可能改善我们管理癌症的方式。我们希望这种药物捕获的概念可以扩展到解决医学中必须应对脱靶毒性的其他问题。”
来源:中国3D打印网
如有侵权,请及时联系删除!








